跨膜蛋白|多次跨膜( CCR8|ABCD1|C5AR1|CD24|CLDN18.2|CD20|AQPZ)
- CSB-005
- 华美CUSABIO
- 湖北省武汉市
- 一周内
- 100ug
- 888 元
- 2022-05-18 15:59:14
武汉华美生物工程有限公司

- 英文名称
- CCR8|ABCD1|C5AR1|CD24|CLDN18.2|CD20|AQPZ protein
- 别名
- CCR8|ABCD1|C5AR1|CD24|CLDN18.2|CD20|AQPZ protein
- 关键词
- 跨膜蛋白靶点蛋白重组蛋白活性蛋白

跨膜蛋白(TP),也称为整合膜蛋白,占膜蛋白总量的70%~80%。其主要特征是不溶于水,其氨基酸组成疏水性强,也有亲水性氨基酸,由疏水性氨基酸组成的部分,深入脂双层的疏水区,与脂肪酸链共价结合,它们可分布在脂双分子层中或跨越全膜。跨膜蛋白在基本生理过程中起着重要作用,包括分子运输、信号转导和能量利用等。一方面,它们可用于向细胞传递外部环境的信号。另一方面,它们充当接收器收集有关外部环境信号。
跨膜蛋白是目前最主要的药物靶点,占现阶段己知药物靶点的60%以上,以跨膜蛋白为靶点的创新药研发一直是医药领域的研究热点。由于跨膜蛋白具有疏水亲脂的跨膜域,必须借助细胞膜的磷脂双分子层这一特殊环境来维持正确结构、保持生物活性,同时跨膜次数越多其具有的疏水亲脂跨膜区越多,在宿主细胞中表达水平越低,制备难度越大,因此体外制备有活性的跨膜蛋白是目前公认的技术难题。
具有全长完整结构的多次跨膜蛋白在药物研发中具有重要意义。为助力跨膜蛋白靶点药物的开发,华美生物在原有大肠杆菌、毕赤酵母、哺乳动物细胞和杆状病毒-昆虫细胞四大表达系统的基础上,开发出表达跨膜蛋白的无细胞和基于哺乳细胞的病毒样颗粒(VLPs)两大核心技术,并成功制备200余种跨膜蛋白,包含CCR8、C5AR1、Claudin-18.2等多个热门靶点。
产品优势
● 多种膜蛋白表达策略
针对跨膜蛋白,华美生物开发出三大优势蛋白表达平台,应用无细胞表达技术结合去垢剂助溶或Nanodisc磷脂层结构技术,哺乳细胞表达结合VLPs技术,帮助跨膜蛋白形成正确的构象,使其具有生物活性,以满足相关研究及检测使用。

病毒样颗粒 (VLPs) 技术平台
VLPs是由多个病毒的一种或者多种衣壳蛋白自动组装形成的纳米级别的微小颗粒。VLPs颗粒不含病毒核酸,不能进行自主复制,安全性高,具有与病毒颗粒类似的整体结构。
华美生物搭建了基于HEK293表达系统的包膜VLPs技术平台,所制备的包膜VLPs在其固有的囊泡膜上显示正确折叠的多次跨膜蛋白,展示完整的生物活性。
去垢剂技术平台
去污剂是同时具有亲水极性基团和疏水非极性基团的双极性分子,能够使脂膜解体释放膜蛋白,并在溶液中为去膜状态下的膜蛋白提供疏水环境,维持膜蛋白的疏水跨膜结构。
华美生物搭建了基于无细胞表达的去垢剂技术平台。通过体外添加DNA模板、ATP、氨基酸、各种底物、细胞抽提物的酶等合成蛋白质,筛选不同去垢剂来提取目的蛋白,可很好溶解纯化跨膜蛋白,帮助其在溶液中形成天然正确构象。
Nanodisc技术平台
在含有去垢剂的缓冲液中,大部分膜蛋白可以维持稳定性和活性。但少数对去垢剂敏感的膜蛋白是不适宜含有去垢剂的缓冲条件的,具体表现为无法纯化,稳定性不好和没有活性。
华美生物搭建了基于无细胞表达的Nanodisc技术平台。通过体外添加MSP,磷脂分子使其在反应过程中边表达边组装成Nanodisc结构,保持其生物学活性并有很好的水溶性。
● 近200种全长跨膜蛋白
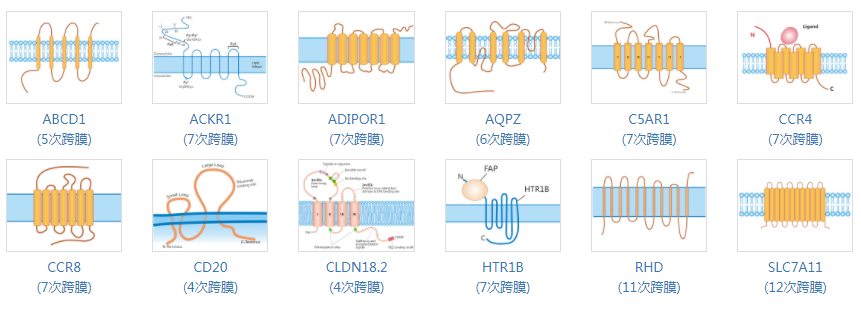
● 多平台验证
华美生物应用WB技术验证跨膜蛋白特异性,采用功能性ELISA/SPR/FACS等多种蛋白应用分析技术验证跨膜蛋白活性,并通过SEM方法验证跨膜蛋白正确组装,确保给客户提供高活性、高纯度、构象正确的全长跨膜蛋白。

Q&A
Q:可否详细介绍下几个平台是如何表达及组装跨膜蛋白的?
A: VLPs平台——包膜病毒衣壳蛋白表达过程中可以自我组装成纳米颗粒,目的蛋白(跨膜蛋白)表达之后定位在细胞膜上,VLP通过出芽的方式释放出去,释放的过程中会和细胞膜整合(细胞膜上有目的蛋白),释放后的纳米颗粒(即VLPs颗粒)包膜上会展示跨膜蛋白。
去垢剂平台——大肠杆菌无细胞表达,之后用去垢剂溶解纯化。
Nanodiscs平台——大肠杆菌无细胞表达过程中添加膜骨架蛋白(MSP)和磷脂分子(DMPC)使其边表达边组装成nanodiscs。
Q: 以上所有平台的膜蛋白制备过程中,是否有用到任何的病毒或者病毒载体?
A:哺乳包膜VLPs即包膜病毒样颗粒,是由病毒一个或几个结构蛋白自行组装成不含病毒基因组且不能复制、不具有感染能力,只是形态结构上类似完整病毒,并不含有病毒核酸物质,是安全的。现在不少疫苗也会选择该技术,可见其是安全的。
Q:Nanodisc平台用的脂质体和膜骨架蛋白分别选择了多少种进行组合,是否针对每个项目优化组合?
A:华美生物在前期平台研发阶段尝试了多种膜骨架蛋白和磷脂分子,进行了正交组合尝试,最终筛出了一对最适的膜骨架蛋白和磷脂分子,可成熟针对不同项目。
文献引用
Recombinant Human C-C chemokine receptor type 8 (CCR8), CSB-CF004847HU
The chemokine CCL1 triggers an AMFR-SPRY1 pathway that promotes differentiation of lung fibroblasts into myofibroblasts and drives pulmonary fibrosis, Immunity, 2021.
Recombinant Mouse Tyrosinase (Tyr), CSB-CF025394MO
Altered T cell subpopulations and serum anti-TYRP2 and tyrosinase antibodies in the acute and chronic phase of alopecia areata in the C3H/HeJ mouse model K Hashimoto, Journal of Dermatological Science, 2021.
Recombinant Mouse CD44 antigen (Cd44), CSB-CF004938MO
Effect of Vitamin B2 and Vitamin E on Cancer-Related Sarcopenia in a Mouse Cachexia Model T Mori, BioMed, 2021.
Recombinant Chicken Follicle-stimulating hormone receptor (FSHR),CSB-CF009021CH
Recombinant Chicken Lutropin-choriogonadotropic hormone receptor (LHCGR), CSB-CF849533CH
MicroRNA-21-containing microvesicles from tubular epithelial cells promote cardiomyocyte hypertrophy Min Yang, Renal Failure, 2021.
Recombinant Escherichia coli Colicin-E1(cea), CSB-CF360926ENL
An ultrasensitive electrochemical sensing platform for the detection of cTnI based on aptamer recognition and signal amplification assisted by TdT M Lang, RSC Advances, 2020.
相关资源
跨膜蛋白介导细胞与细胞外环境间的信号传导,并执行许多重要的细胞生物学功能。例如,它是各种信号分子、激素和其他底物的受体;它参与细胞膜内部和外部之间物质、能量和信号的交换;它构成了各种离子跨膜的通道,该通道将营养物质和一些无机电解质输入细胞,并将有毒或无用的代谢产物排放到细胞中。
由于无细胞表达系统的独特优势,它们在跨膜蛋白表达中起着重要作用。
在无细胞表达系统中,我们可以修饰跨膜蛋白。比如可以将非天然氨基酸添加到蛋白质表达中,以实现在常规重组表达后难以解决的复杂修饰过程。
由无细胞表达系统表达的跨膜蛋白产物可用于研究跨膜蛋白的功能。跨膜蛋白整合到囊泡中进行结构和功能研究是膜蛋白研究的热门话题。
无细胞表达系统表达的跨膜蛋白类型和功能是多种多样的。目前热销的跨膜蛋白包含以下几类:




| 华美生物︱YOUR GOOD PARTNER IN BIOLOGY RESEARCH! | |
| 武汉华美生物工程有限公司成立于2007年12月,是一家集科研、生产、销售为一体的生物高新技术企业。并形成了以CUSABIO为品牌的ELISA试剂盒、外泌体提取试剂盒、蛋白、抗体等多种优质产品,远销欧美日德等九十多个国家。 推荐您微信关注华美官方公众号,方便查询产品,同时获取生命科学更新资讯! |
|