云序用户 1区,IF=23.168 | 多组学联合分析揭示胰腺癌中 RNA 乙酰化修饰的重要靶点
近期,云序客户上海交通大学医学院附属瑞金医院研究者们在血液肿瘤领域的高分专业期刊Journal of Hematology & Oncology (IF=23.168)上发表了一篇多组学联合分析的分子功能机制研究论文,详细阐释了胰腺导管腺癌当中的一个长链非编码 RNA 通过调控 mRNA 乙酰化来影响关键致癌基因的蛋白翻译效率的致癌机制,并基于该理论提出了胰腺导管腺癌诊断和治疗的新思路。云序生物有幸参与了本次研究当中的acRIP-seq、mRNA-seq 、Ribo-seq以及生信分析。

论文链接:The LINC00623/NAT10 signaling axis promotes pancreatic cancer progression by remodeling ac4C modification of mRNA
发表期刊:Journal of Hematology & Oncology (IF=23.168)
作者院校:上海交通大学医学院附属瑞金医院
核心方法:RIP-seq、acRIP-seq、mRNA-seq 、Ribo-seq、外泌体 lncRNA 测序、RNA pulldown+蛋白质谱、co-IP
1、LINC00623 是胰腺癌患者血清外泌体中的分子标志物
作者取 5 位胰腺导管腺癌(pancreatic ductal adenocarcinoma,PDAC,后文简称胰腺癌)患者以及 5 位健康人的血清,分离血清外泌体,并进行外泌体 lncRNA 测序。其中,作者发现了 180 个在胰腺癌患者中显著上调的 lncRNA,148 个显著下调的 lncRNA。研究者在公开数据库中获取了胰腺癌细胞系和组织中 lncRNA 的表达水平,从而在前述的 180 个上调 lncRNA 当中选出了 2 个候选者:LINC00623 和 HOXA-AS2——它们在胰腺癌细胞系、组织以及血清外泌体当中均发生了上调。
研究者随后在血清外泌体样品中使用 RT-qPCR 方法验证了 LINC00623 这个 lncRNA 在胰腺癌与健康人之间的巨大差异。然而,血清外泌体样品的 RT-qPCR 并未显示 HOXA-AS2 这个 lncRNA 在胰腺癌与其它胰脏疾病之间的显著差异。因此,作者选取了 LINC00623 这个 lncRNA 进行后续的研究。
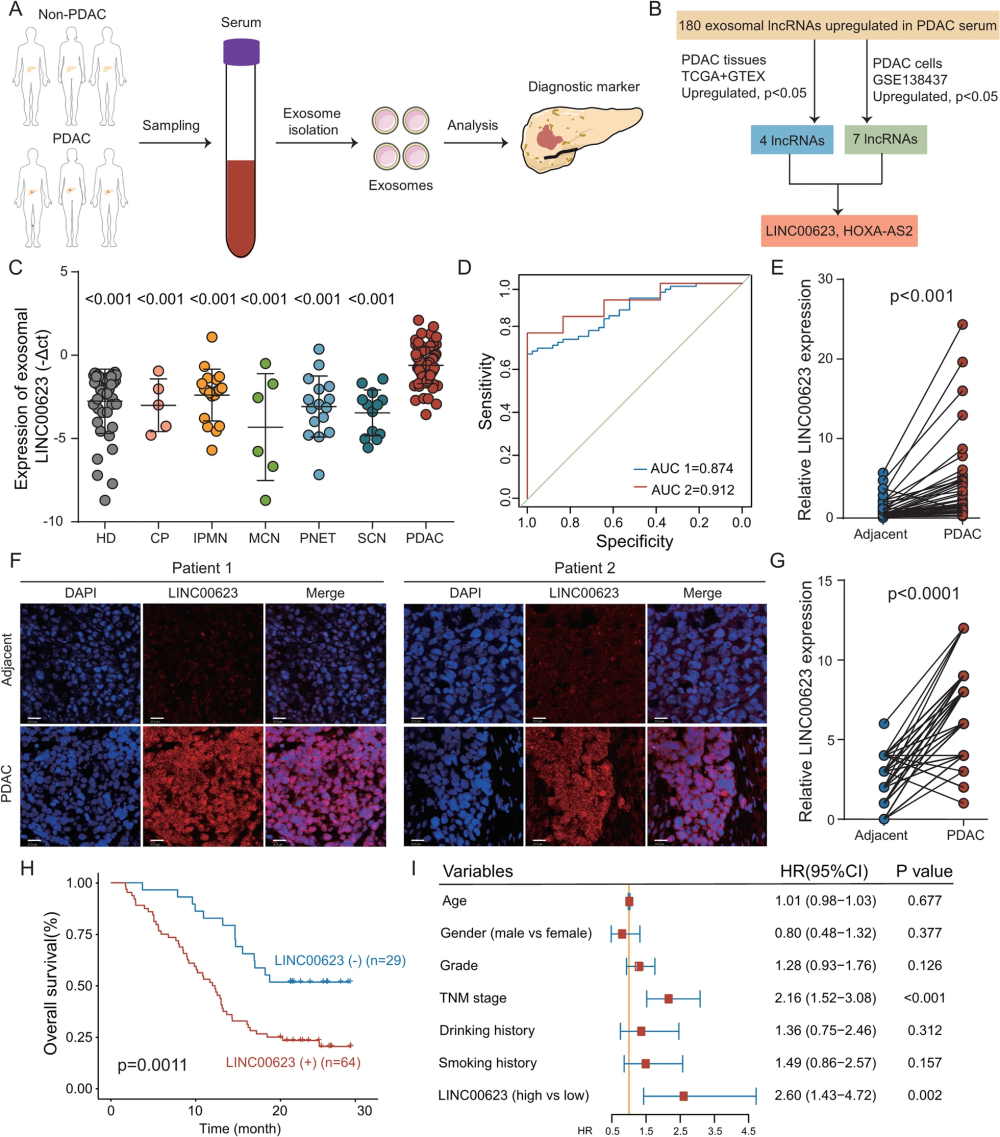
一系列实验和统计结果显示,血清外泌体 LINC00623 可以作为分子标志物有效区分胰腺癌患者与健康人(AUC 接近 0.9),并且可以在体外细胞实验以及小鼠体内实验当中促进胰腺癌的肿瘤发生以及转移。
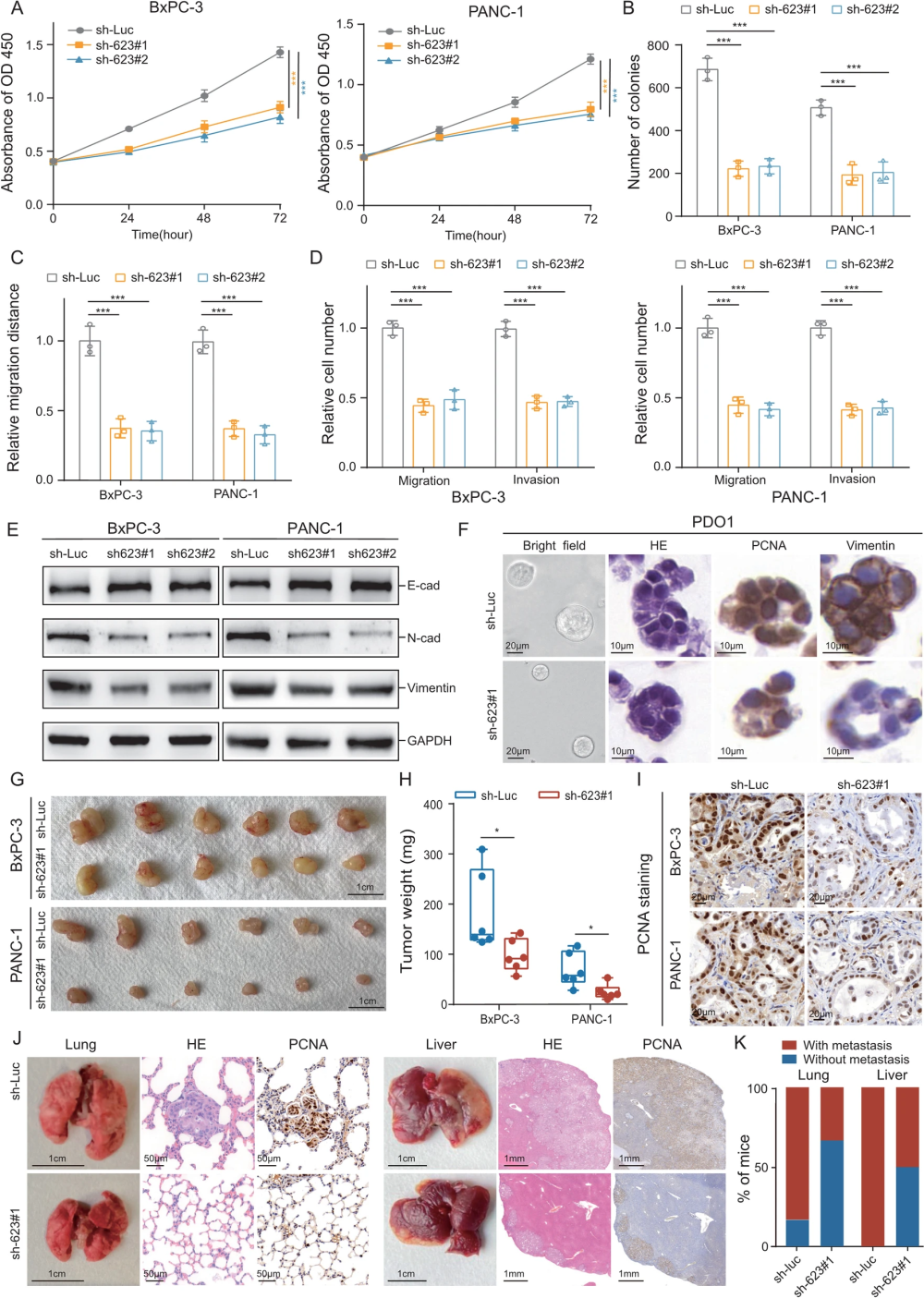
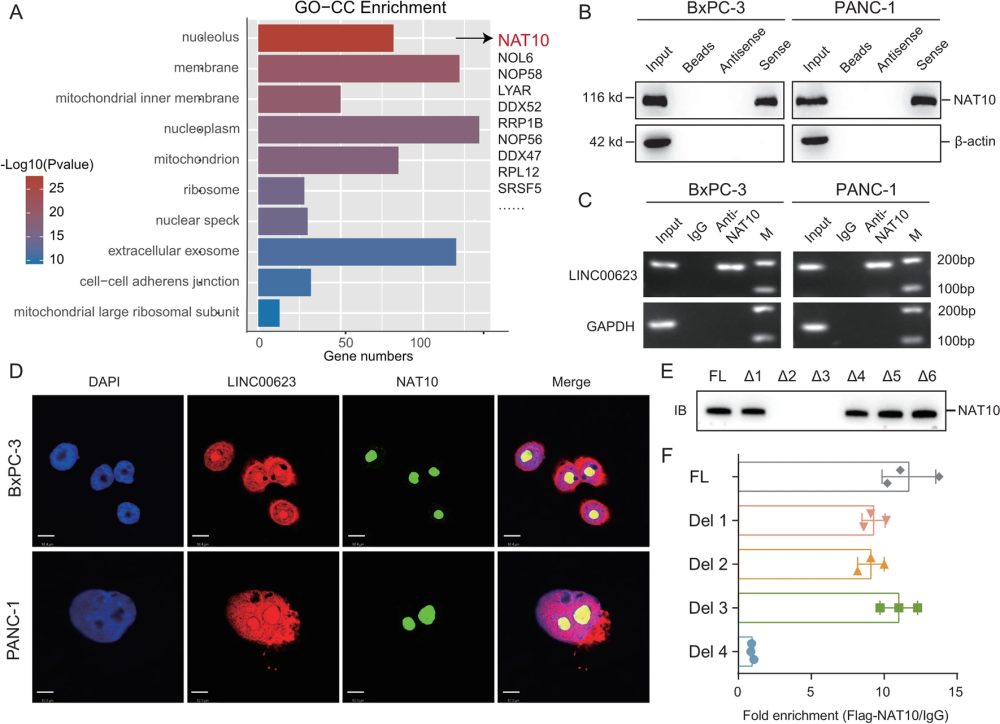
2、LINC00623 与 ac4C 乙酰化酶 NAT10 结合
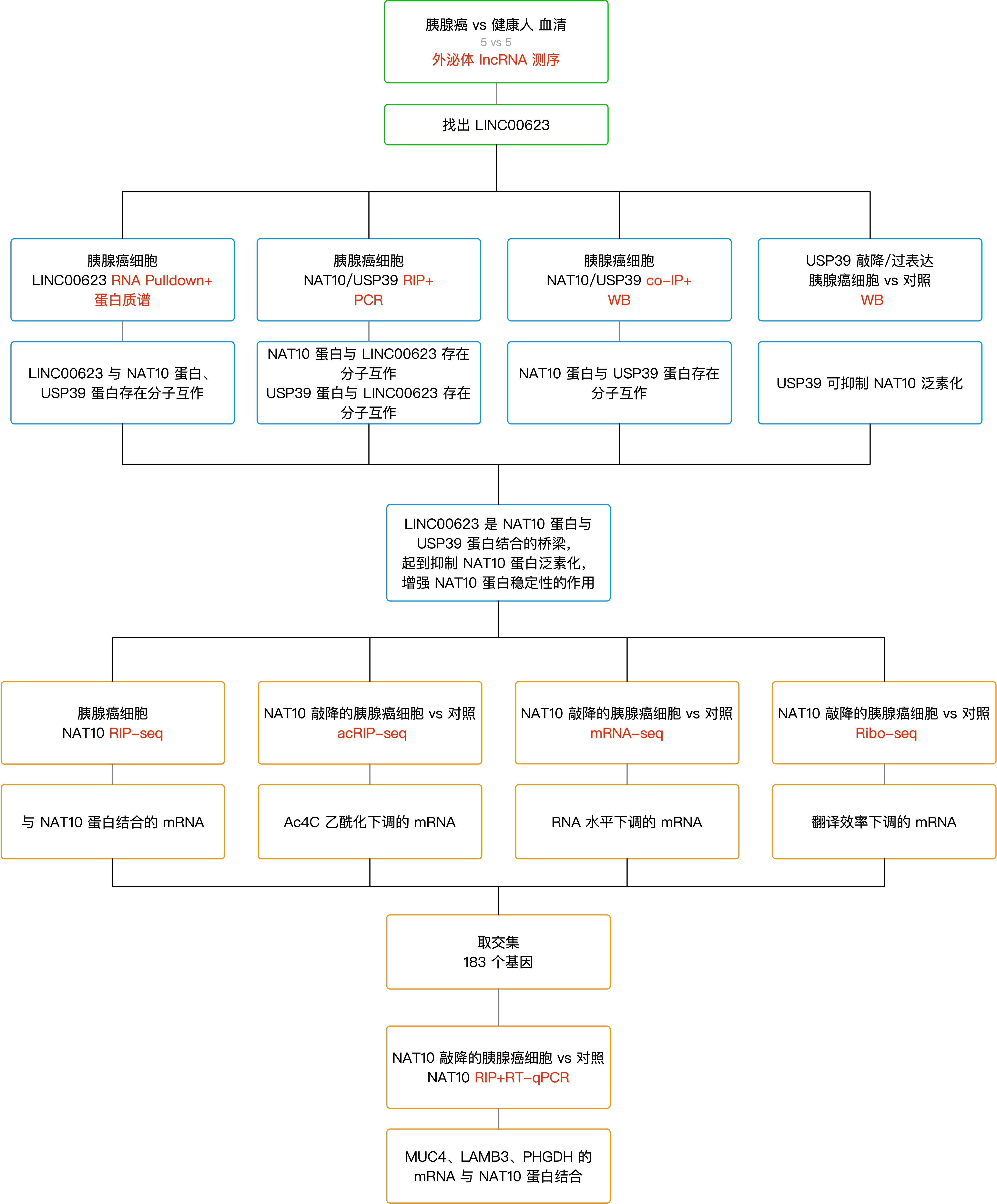
由于 lncRNA 的生物学功能与其分布的亚细胞结构息息相关,作者随后对 LINC00623 进行了 FISH 实验,证明大部分的 LINC00623 分布于细胞核当中,因此作者猜测它可能与细胞核内的蛋白发生互作。随后,作者针对 LINC00623 进行了RNA pulldown+蛋白质谱,发现了 433 个与 LINC00623 存在分子互作的蛋白质,其中之一就是 RNA ac4C 乙酰化修饰的 Writer 蛋白 NAT10。为了验证 NAT10 与 LINC00623 的分子互作,作者进行了针对 NAT10 蛋白的 RIP 实验,果然在 RIP 结合产物中通过 PCR 发现了 LINC00623 的存在。作者更进一步还进行了一系列突变和删除实验,确定了 LINC00623 的 700-1800 nt 区间是与 NAT 10 蛋白结合的区域,而 NAT10 蛋白上的 753-1025 aa 区间则是与 LINC00623 lncRNA 结合的区域。
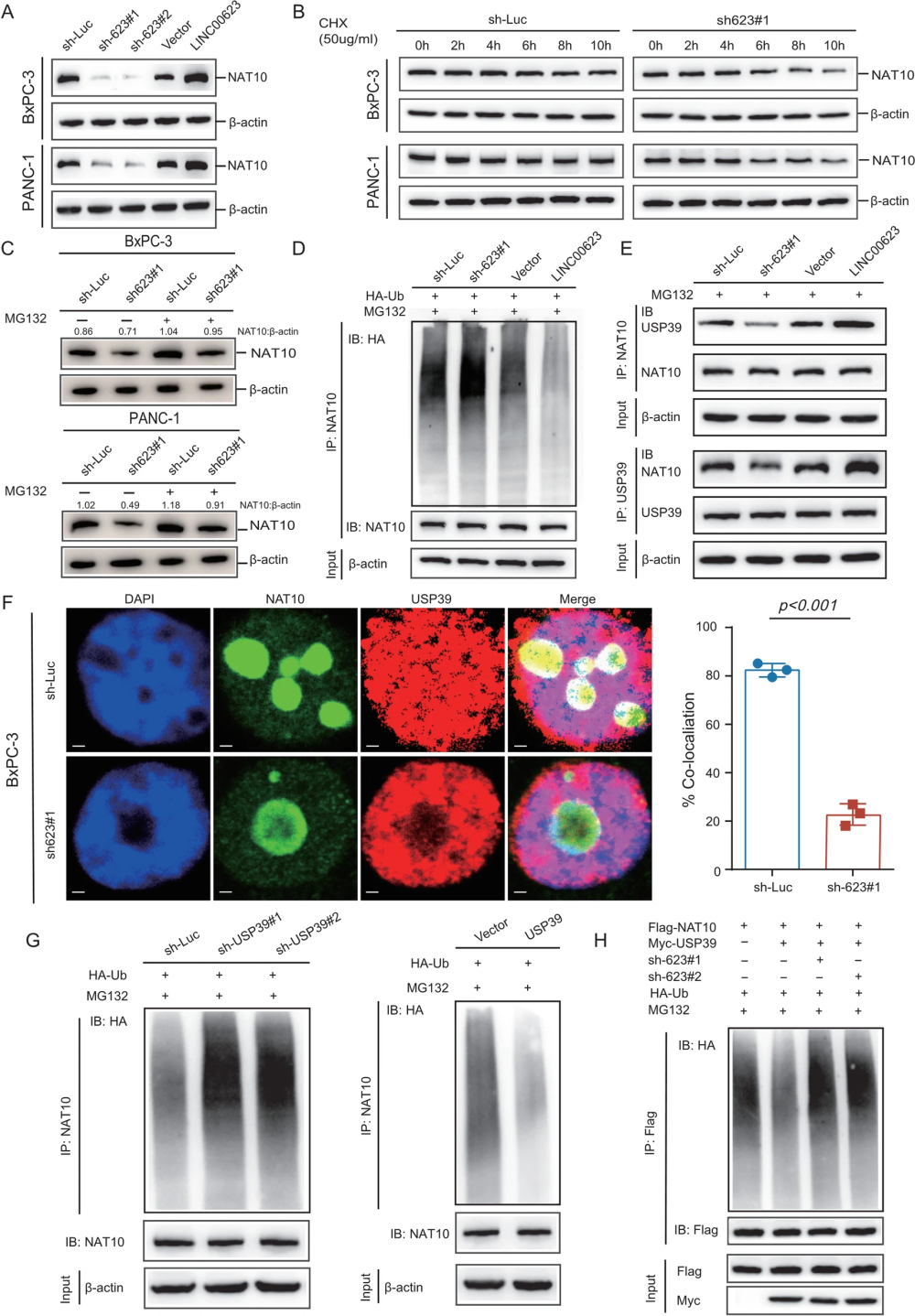
3、LINC00623 可以阻断 NAT19 的泛素化和降解
作者接下来想要探究 LINC00623 如何调控 NAT10 的分子功能。作者发现 LINC00623 虽然并不影响 NAT10 在 mRNA 水平的表达量,但是 LINC00623 的过表达/敲降却可以显著提升/降低 NAT10 的蛋白质水平。并且,在翻译抑制剂 CHX 的作用下,敲降 LINC00623 还能降低 NAT10 蛋白的半衰期。研究者于是怀疑 LINC00623 可能可以调控 NAT10 蛋白的泛素化降解。实验结果显示,蛋白酶体抑制剂 MG132 果然可以使 LINC00623 敲降细胞的 NAT10 蛋白水平由低转高。作者还检测了 NAT10 蛋白的泛素化水平,也发现 LINC00623 过表达/敲降细胞的 NAT10 泛素化水平下降/上升。这些证据都证明,LINC00623 这个 lncRNA 通过抑制 NAT10 蛋白的泛素化,来阻断其被蛋白酶体降解的过程,从而起到维持 NAT10 蛋白的作用。
那么,LINC00623 究竟是如何抑制 NAT10 蛋白的泛素化的呢?先前针对 LINC00623 的RNA pulldown+蛋白质谱 实验当中发现了 433 个与 LINC00623 结合的蛋白质,其中有两个去泛素化酶 USP39 和 PRRF8。先前有文献报道发现,NAT10 蛋白与 USP39 蛋白会发生免疫共沉淀。因此,作者提出假说,认为 LINC00623 是 NAT10 蛋白与 USP39 蛋白结合的桥梁。作者随后做了针对 USP39 蛋白的 RIP 实验以及针对 LINC00623 的 RNA pulldown 实验,证明了 USP39 蛋白与 LINC00623 之间确实存在分子互作。并且,co-IP 实验也证明,在 LINC00623 存在的前提条件下,USP39 蛋白与 NAT10 蛋白存在分子互作。随后研究者对 NAT10 蛋白上的泛素蛋白 HA-Ub 进行了检测,发现泛素蛋白 HA-Ub 的水平与 USP39 负相关。综合多个实验的结果,作者得出结论:LINC00623 是 NAT10 蛋白与 USP39 蛋白结合的桥梁,通过阻断 NAT10 蛋白的泛素化降解来增强其蛋白质稳定性。
4、LINC00623 通过 NAT10 调控 mRNA 的 ac4C 修饰
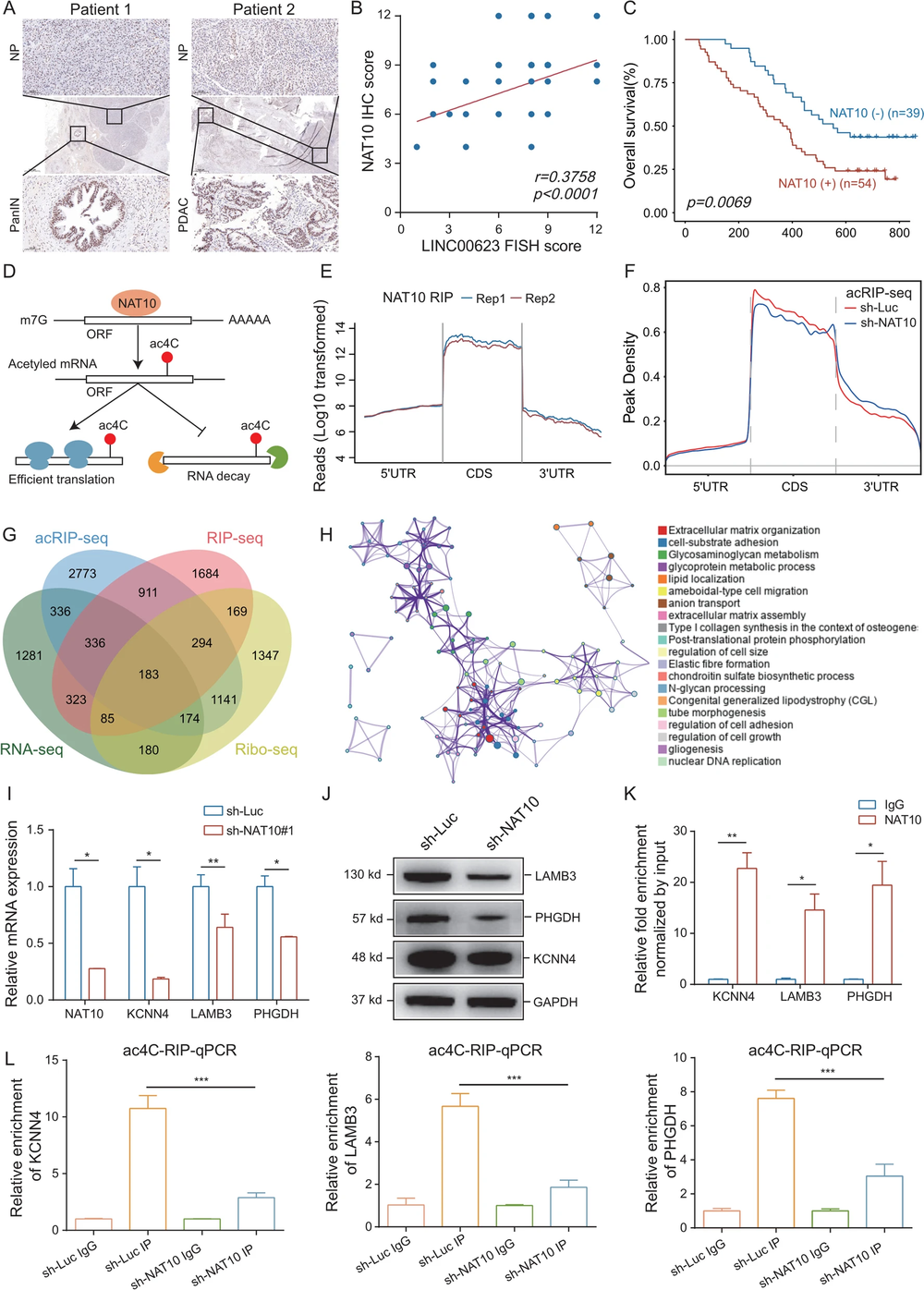
研究者在93对胰腺癌病人的癌组织和癌旁组织之间进行免疫组化实验,验证了 NAT10 蛋白水平在胰腺癌组织当中的上调,并且免疫组化测得得 NAT10 蛋白水平与 FISH 测得的 LINC00623 的 RNA 水平之间存在正相关关系。在作者的研究队队列或者公开数据库的病历当中,高 NAT10 蛋白水平都与更低的患者生存率有关。
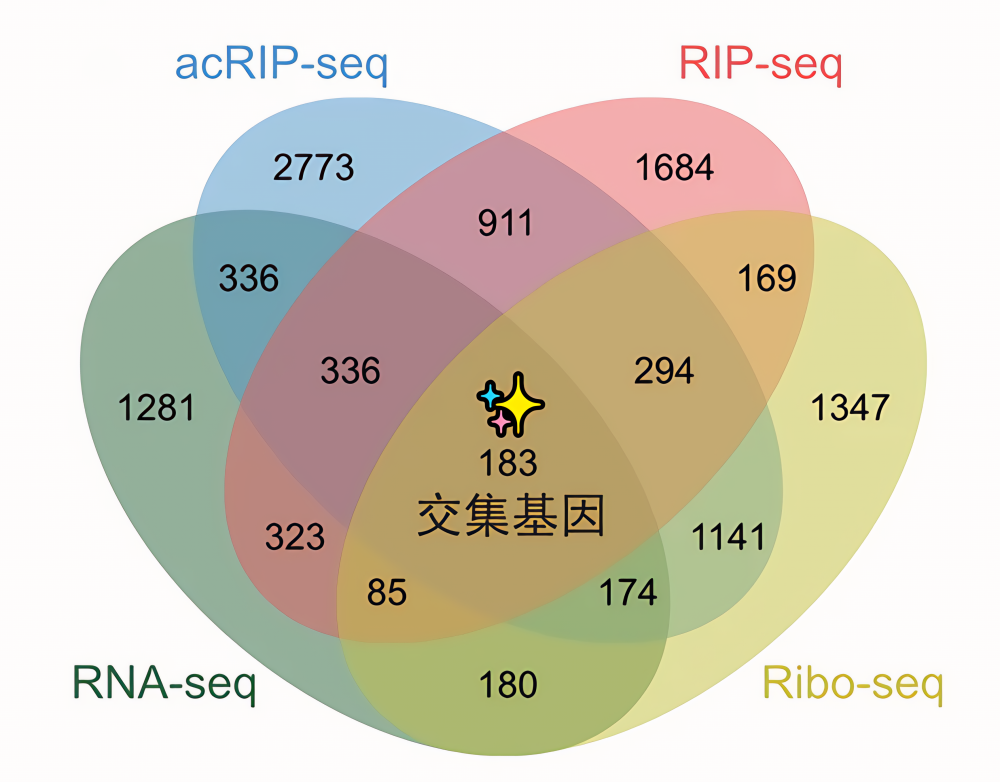
NAT10 是目前已知的唯一一个 RNA 的 ac4C 乙酰化酶(即 ac4C “Writer”蛋白)。作者在 NAT10 敲降的细胞当中,进行了 NAT10 RIP-seq、acRIP-seq、mRNA-seq 以及 Ribo-seq。NAT10 RIP-seq 以及 acRIP-seq 的结果显示,NAT10 以及 ac4C 修饰广泛分布于整个转录组上,且主要集中分布于 CDS 区。此外,作者对以下4个基因集做了取交集的处理:
1. NAT10 RIP-seq 富集到的基因集;
2. acRIP-seq 当中,在 NAT10 敲降细胞与对照细胞之间乙酰化修饰显著下调的 mRNA 所对应的基因集;
3. mRNA-seq 当中,在 NAT10 敲降细胞与对照细胞之间 RNA 水平显著下调的 mRNA 所对应的基因集;
4. Ribo-seq 当中,在 NAT10 敲降细胞与对照细胞之间翻译效率显著下调的 mRNA 所对应的基因集。
以上这 4 个基因集的交集当中,有 183 个基因,其中 12个 基因已知与胰腺癌的病程密切相关。由这 183 个交集基因出发所作的 GO 分析显示,这些基因富集于细胞生长(Cell growth)、细胞粘附(Cell adhesion)和细胞外基质(Extracellular matrix organization)有关的条目当中。RT-qPCR 和 Western blotting 结果显示,在 LINC00623 敲降的细胞当中,UMUC4、LAMMB3、PHGDH 等基因在 mRNA 水平和蛋白质水平上均显著下降。针对 NAT10 的 RIP 实验后接 RT-qPCR 显示,MUC4、LAMB3、PHGDH 等 ac4C 修饰的 mRNA 确实存在与 NAT10 蛋白的分子互作。综合各种实验的结果,作者认为 LINC00623 对胰腺癌的作用依赖于 NAT10,它重塑了胰腺癌中的 ac4C 修饰谱,维持了一系列致癌 mRNA 的稳定性,并促进其翻译效率。
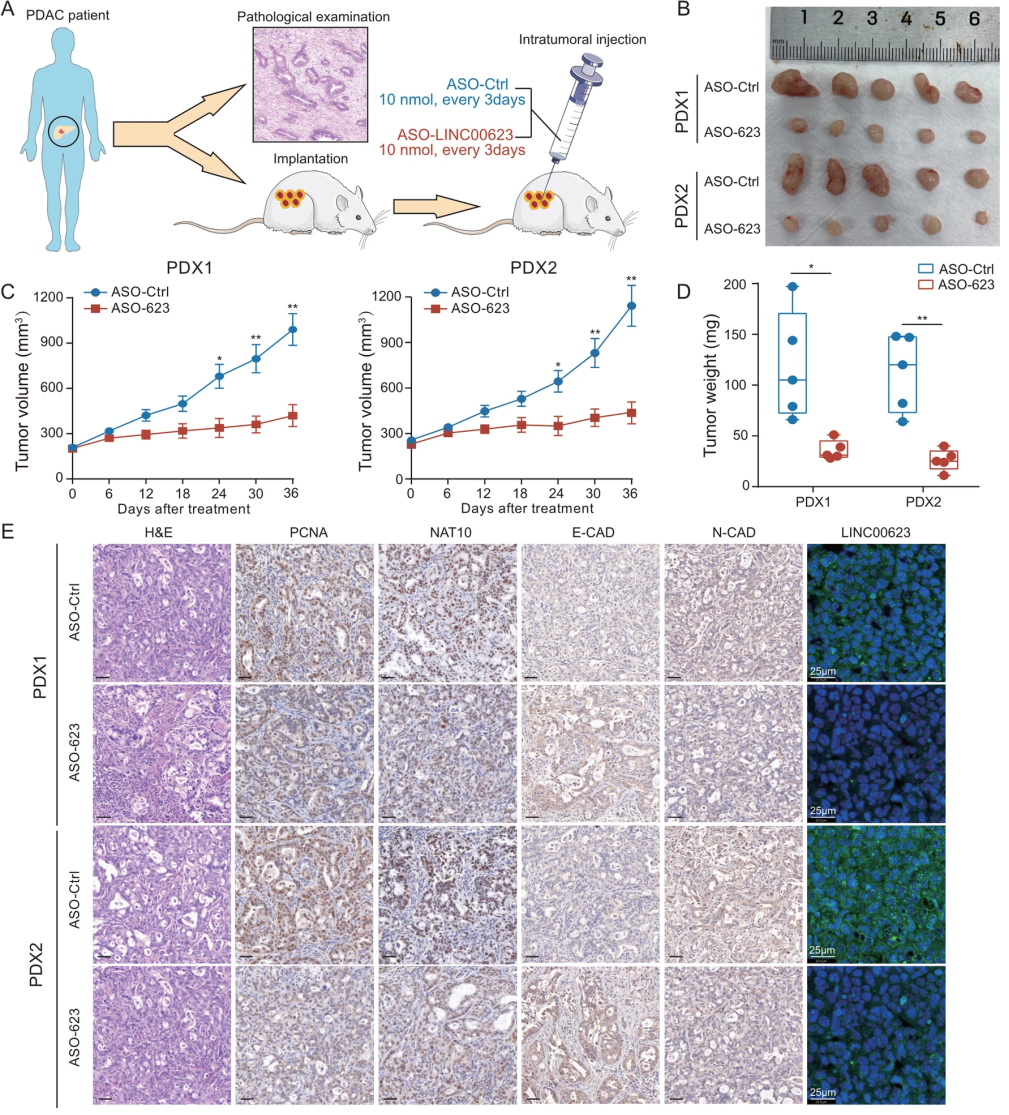
5、LINC00623 是胰腺癌的潜在治疗靶点
由于 LINC00623 在胰腺癌中起着至关重要的作用,作者进一步研究了 LINC00623 作为胰腺癌的治疗靶点的可能性。研究者用新鲜的胰腺癌组织建立了患者来源的异种移植(Patient-derived xenograft,PDX)模型。该模型具有较高的LINC00623表达水平。研究者将 LINC00623 的体内优化抑制剂(ASO-LINC00623)通过瘤内注射给 PDX 模型,结果显示 ASO-LINC00623 明显减少了两个 PDX 模型的肿瘤负担。并且,该疗法对来自 LINC00623 表达较高的胰腺癌组织的肿瘤有较大的改善效果。随后,作者对 PDX 进行 H&E 和免疫组化染色,结果显示 ASO-LINC00623 明显降低了 LINC00623 的表达,减弱细胞增殖,降低上皮-间充质转化(Epithelial to mesenchymal transition,EMT),而这一切都可能要归功于 NAT10 的蛋白水平下降。综上所述,LINC00623 是一个很有潜力的胰腺癌治疗靶点。
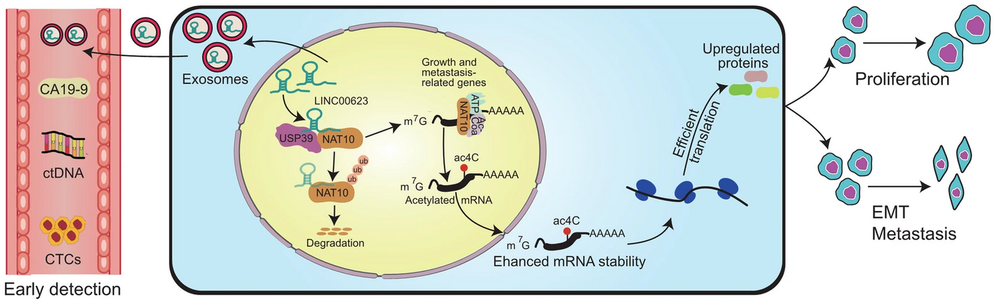
胰腺癌患者的血清外泌体当中的 lncRNA LINC00623 可以作为诊断的生物标志物,对早期胰腺癌的诊断具有高特异性和敏感性。LINC00623/NAT10信号轴促进胰腺癌细胞的增殖、致瘤、迁移和侵袭能力。作者巧妙运用 NAT10 RIP-seq、acRIP-seq、mRNA-seq 以及 Ribo-seq 进行联合分析,阐释了 NAT10 通过重塑 mRNA 的 ac4C 修饰谱、增强致癌 mRNA 的稳定性和翻译效率的分子机制:LINC00623 可通过阻断泛素化来增强 NAT10 蛋白的稳定性,进而促进 UMUC4、LAMMB3、PHGDH 等致癌基因的 mRNA 发生 ac4C 修饰,增强 mRNA 水平,提升蛋白质翻译效率。基于以上发现,一种针对 LINC00623 的抑制剂 ASO-LINC00623 很有可能成为治疗胰腺癌的新药。
01 ac4C RNA修饰测序
ac4C RNA修饰测序
对ac4C RNA乙酰化,目前最流行的检测手段为acRIP-seq技术,适用于ac4C RNA乙酰化谱研究,快速筛选ac4C RNA乙酰化靶基因。云序可提供mRNA和多种非编码RNA的ac4C测序:
- ac4C 全转录组测序(涵盖mRNA,LncRNA,circRNA)
- ac4C LncRNA测序(涵盖LncRNA和mRNA)
- ac4C Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
- ac4C mRNA测序
- ac4C rRNA测序
- ac4C tRNA测序
02 检测整体ac4C RNA修饰水平
LC-MS/MS检测整体RNA修饰水平
精准高效,可以实现一次检测55类修饰水平检测,一步到位。
03 ac4C RNA修饰上游酶的筛选
ac4C RNA修饰相关酶PCR芯片
寻找上游直接调控ac4C RNA乙酰化的甲基转移酶。
04 ac4C RNA修饰靶基因验证
acRIP-qPCR
云序提供acRIP-qPCR服务,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证靶基因RNA修饰水平。
05 机制互作研究
RIP-seq/qPCR
筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
筛选或验证目标蛋白与DNA互作,研究相应的分子调控机制。
相关产品
m5C RNA甲基化测序
m1A RNA甲基化测序
ac4C RNA乙酰化测序
O8G RNA氧化修饰测序
2’-O-RNA甲基化测序
m6Am RNA甲基化测序
LC-MS检测整体ac4C甲基化水平
RNA修饰相关酶PCR芯片
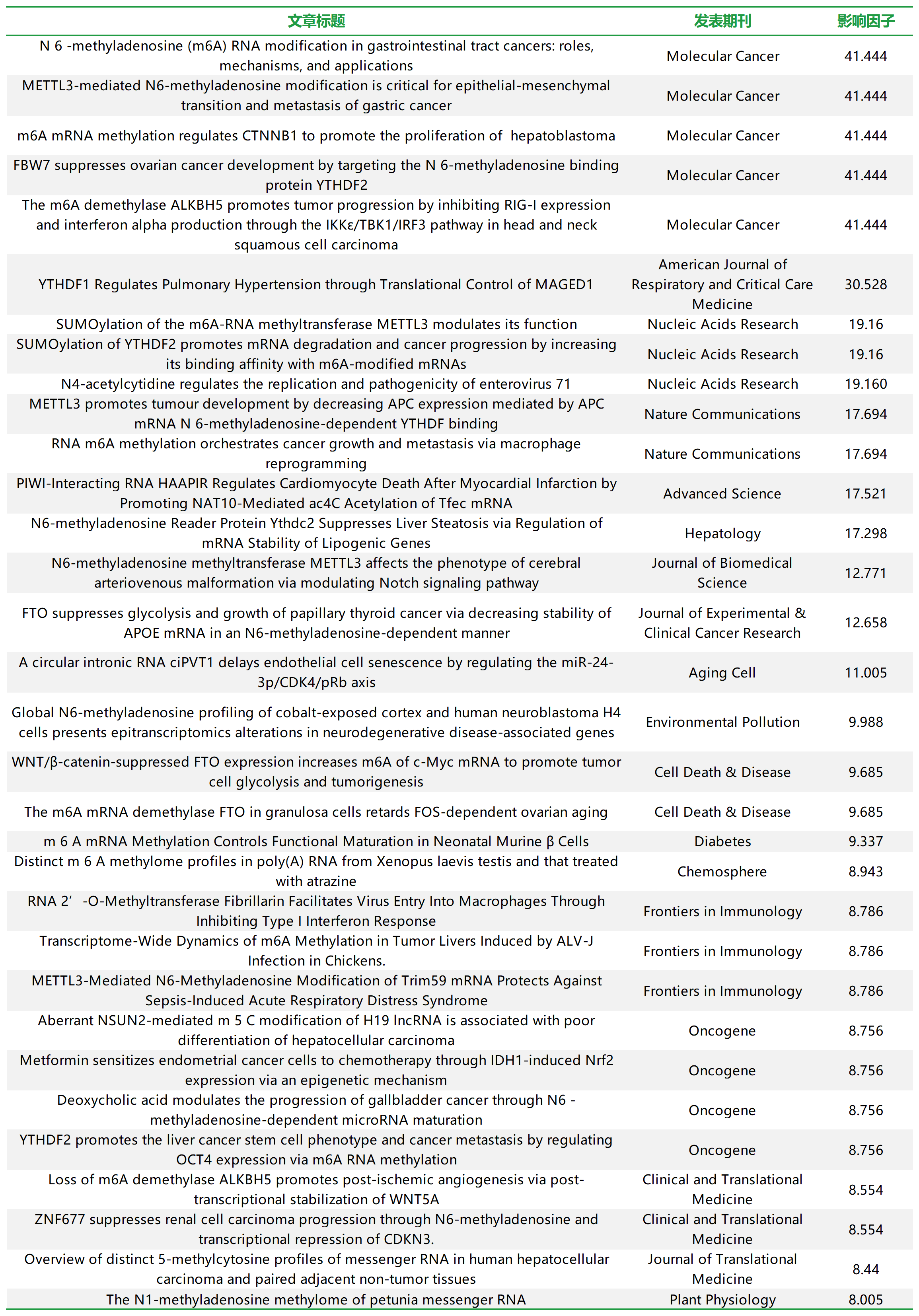
往期回顾
1区,IF=19.16| 云序RNA乙酰化测序acRIP-seq助力病毒复制机制研究!
1区,IF=16.8| 云序RNA乙酰化测序/acRIP-seq助力心梗机制研究!
客户文章1区IF 12+ |m6A甲基化测序助力FTO抑制PTC糖酵解代谢机制研究
客户文章|m6A甲基化测序助力脓毒症诱导的ARDS表位机制研究
客户文章|新型RNA修饰之m7G揭示急性髓系白血病发病机制
Nature 新发现:线粒体 m5C 修饰竟是肿瘤转移的元凶!
超详细图文版:如何实现m6A测序数据可视化?
咨询
- 892
- 点赞
- 复制链接
- 举报