
糖尿病小鼠模型
- OB/OB
- 百奥动物
- 江苏省南通市
- 现货
- 按需
- 议价
- 2025-05-28 14:29:36
百奥赛图江苏基因生物技术有限公司
- 关键词
- 自发性糖尿病模型STZ诱导糖尿病模型饮食诱导糖尿病模型
在现代社会,糖尿病已如同隐匿在暗处的“甜蜜杀手”,悄无声息地威胁着全球数以亿计人的健康。国际糖尿病联合会(IDF)发布的数据令人触目惊心,2024年全球约有5.89亿成年人患有糖尿病,这一数字意味着每9个人中就有1人被糖尿病困扰,而其中90%以上为2型糖尿病。据预测,到2050年,全球糖尿病患者人数将突破8.53 亿。在我国,糖尿病的形势同样严峻,发病率约为11.2%,患者总数高达1.2亿左右,且发病年龄呈年轻化趋势。
糖尿病带来的危害是全方位且极其严重的。长期高血糖如同腐蚀剂,会对眼睛、神经、肾脏、心脏、血管等多器官组织造成不可逆的损伤,引发一系列可怕的并发症:糖尿病肾病、视网膜病变、糖尿病足等。同时,糖尿病患者患心血管疾病风险比一般人群高2 - 4倍,心梗、脑梗等心脑血管意外威胁生命健康。
从1921年胰岛素的发现开启了糖尿病药物治疗的先河,到经典的双胍类药物,再到如今GLP1受体激动剂、DPP-4抑制剂和SGLT-2抑制剂等新型药物崭露头角,不仅显著降低血糖,还兼具减重、心血管保护及肾脏保护等多重获益。然而,糖尿病药物的研发仍面临挑战:如何进一步优化药物的心血管代谢获益?如何针对不同患者群体(如肥胖、心肾高风险)制定个体化方案?
针对糖尿病的研究和新药开发的需求,百奥赛图建立了稳定的糖尿病相关指标检测技术,并构建了自发性糖尿病模型B-ob/ob、STZ诱导糖尿病模型、HFD诱导DIO模型以及B-hGLP1R、B-hGCGR等人源化小鼠,这些模型是糖尿病相关药物药效评价的有力工具,能够助力全球糖尿病药物研发。
糖尿病疾病模型
自发性糖尿病模型
ob/ob小鼠是一种自发性糖尿病模型,在生物学特性和生理生化指标上与人类2型糖尿病患者高度相似。与之相关的瘦素(Leptin) 是一类能够抑制食欲,增加能量消耗,抑制脂肪合成促进其分解的肽类激素,其基因突变导致严重肥胖和胰岛素抵抗,因此这种模型并不适用于依赖瘦素信号通路的靶点研究。百奥赛图通过敲除该基因2、3号外显子制备得到B-ob/ob小鼠,具有明显的肥胖症和高血糖症状,是研究高血糖和肥胖症的有力模型。
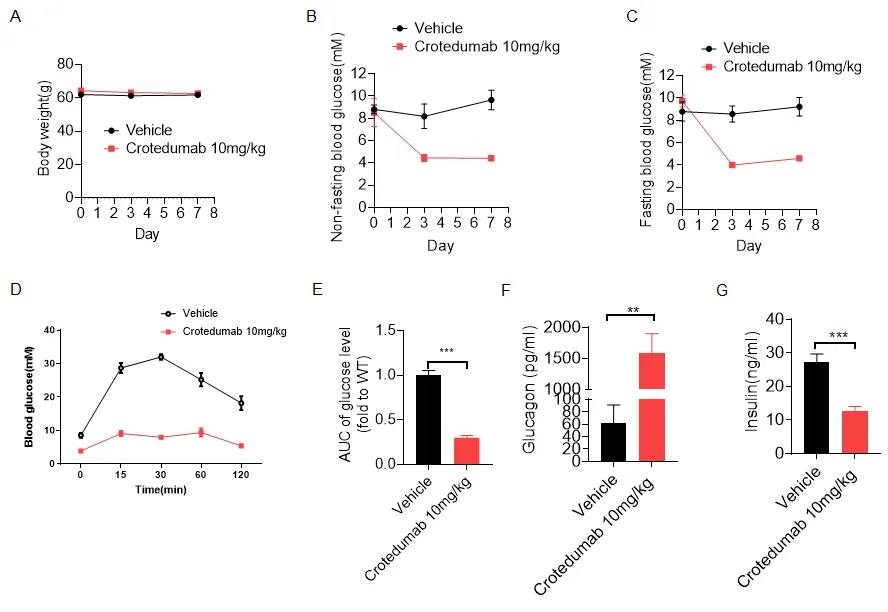
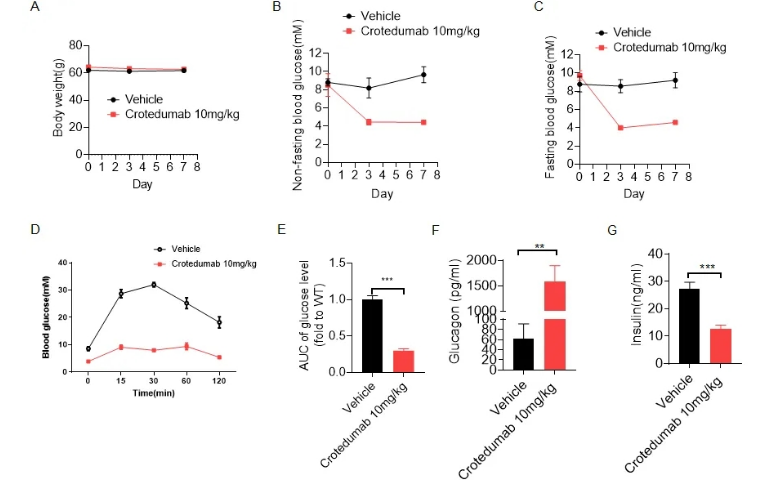
图1:抗人 GCGR 抗体药物 crotedumab 在 B-ob/ob 小鼠中的疗效
(A)B-ob/ob 小鼠的体重变化。(B-C)非空腹血糖和空腹血糖测量(n=6-7)。将 8-10 周龄的雄性 B-ob/ob 小鼠随机分为 2 组,每组 6-7 只动物。给药发生在第 0 天。在第 0 天、第 3 天和第 7 天测量非空腹血糖,空腹 6 小时后测量空腹血糖。(D-E)Crotedumab 给药后葡萄糖耐量测试及曲线下面积。(F-H)胰高血糖素和胰岛素测量。数据以平均值 ± SEM表示。*p<0.05,**p<0.01,***p<0.001。
类似的自发性糖尿病模型还有db/db小鼠。其瘦素受体基因发生突变,使它们无法正常感知瘦素信号,从而表现出暴饮暴食、肥胖、高胰岛素血症和高血糖症等症状,常用于研究 2 型糖尿病的发病机制以及相关药物。
STZ诱导糖尿病模型
链脲佐菌素(STZ)是糖尿病模型最为常用的化学诱导剂。这是一种特异性破坏胰岛β细胞的抗生素,会导致胰岛素分泌不足,血糖升高,广泛用于构建1型糖尿病模型。这种造模方式周期短,可以通过调整诱导剂的剂量和频率来控制糖尿病的发病程度和进程:大剂量单次给药时对胰岛β细胞的杀伤性较强,小鼠消瘦,血糖升高明显,可模拟人类1型糖尿病的发病过程;小剂量多次注射STZ,则更偏向于人类2型糖尿病的特征。
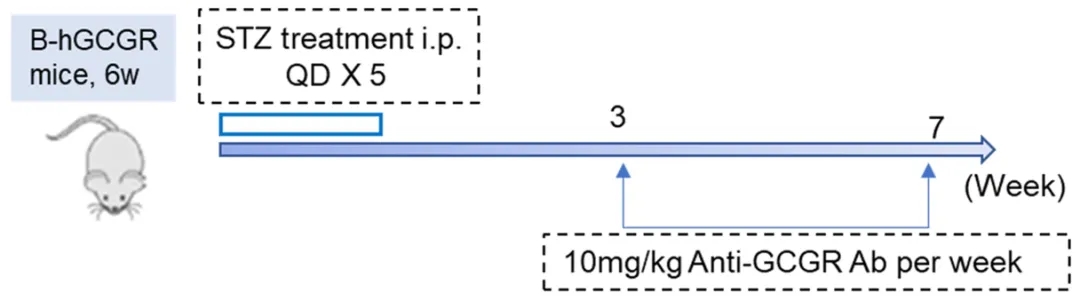
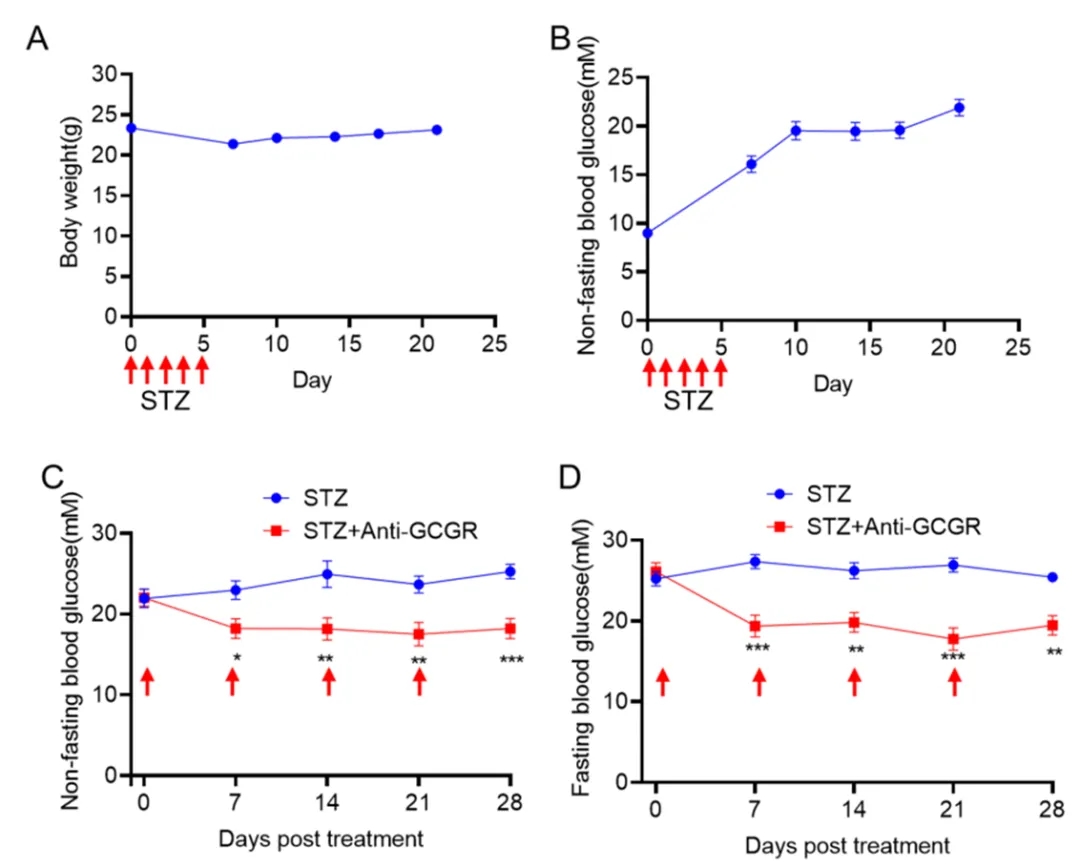
图2:抗GCGR抗体在STZ诱导的B-hGCGR糖尿病小鼠中的体内药效研究
(A-B)STZ诱导的B-hGCGR小鼠的体重和血糖变化。(C-D) STZ诱导3周后,每周一次给药GCGR抗体(10mg/kg,内部合成),测定非空腹血糖(C)和空腹血糖(D) (n = 8)。数据以平均值 ± SEM表示。*p<0.05,**p<0.01,***p<0.001。
饮食诱导肥胖及糖尿病模型
通过给予动物长期的高脂、高糖饮食,诱导肥胖小鼠模型(DIO,Diet-induced Obese),伴随高血糖表现。例如喂食高脂的HFD(High-fat diet),导致动物体重增加、脂肪堆积,逐渐出现胰岛素抵抗现象。胰岛素抵抗意味着身体细胞对胰岛素的敏感性降低,即使体内分泌了正常量的胰岛素,也无法有效地将血液中的葡萄糖转运到细胞内进行利用,从而导致血糖升高,最终诱导糖尿病的发生。这种模型能较好地模拟人类因不良饮食习惯导致的2型糖尿病。
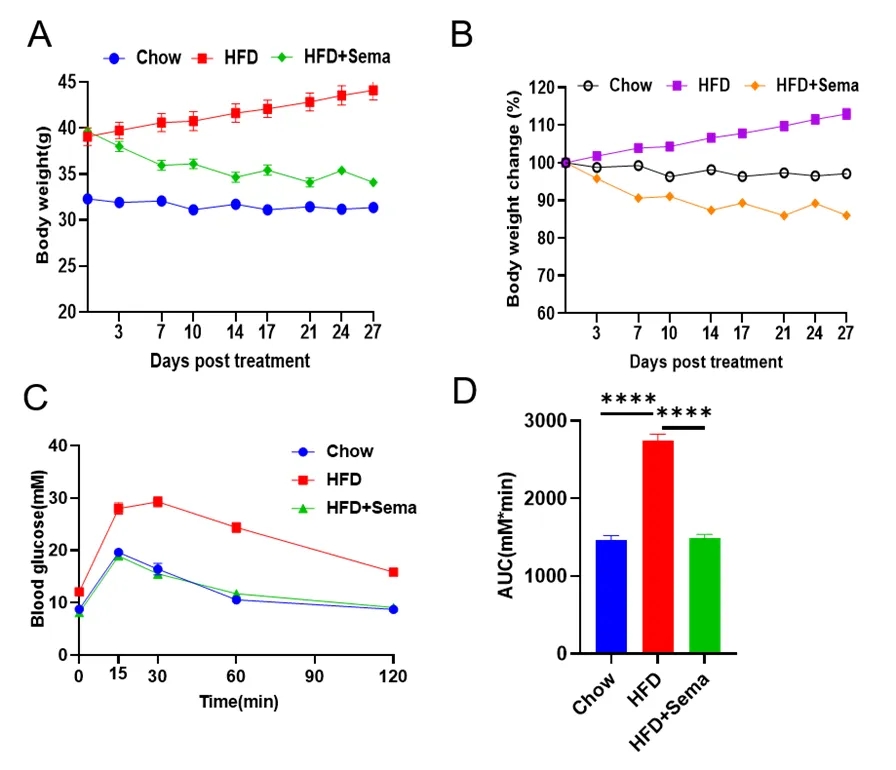
图3:Semaglutide在HFD诱导的DIO小鼠中的体内药效研究。
HFD诱导12周的DIO小鼠,Semaglutide每周三次皮下注射给药,连续给药4周。(A-B) 给药后DIO小鼠的体重变化(n = 10)。(C-D)葡萄糖耐量测试及曲线下面积。数据以平均值 ± SEM表示。*p<0.05,**p<0.01,***p<0.001。
除了以上糖尿病模型外,针对不同机制靶点,百奥赛图还研发了多种热门靶点人源化小鼠用于糖尿病模型的诱导,解决了人源药物与小鼠靶点无法交叉识别的问题,可以有效评估人源治疗药物的药效。
糖尿病靶点人源化小鼠
GLP1R与B-hGLP1R mice
胰高血糖素样肽1(GLP1)是人体胃肠道黏膜天然分泌的一种“肠促胰素”,可以与胰岛细胞上的受体结合并刺激胰岛素分泌,进而降低血糖,同时还可以减少食物摄取和延缓胃排空,有利于控制体重。利用人源化B-hGLP1R小鼠诱导的肥胖及糖尿病模型可检测GLP1R激动剂类药物的药效。
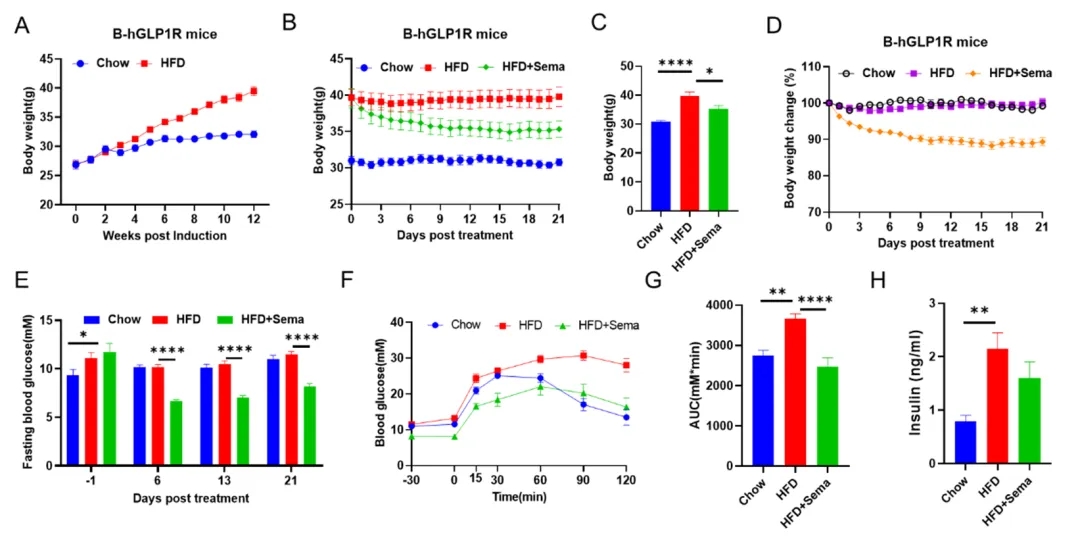 图4:Semaglutide在HFD诱导的B-hGLP1R小鼠中的体内药效研究
图4:Semaglutide在HFD诱导的B-hGLP1R小鼠中的体内药效研究
(A)HFD诱导后的体重变化。(B-D)HFD诱导12周的B-hGLP1R小鼠,Semaglutide每天一次皮下注射给药,连续给药3周。Semaglutide治疗后体重变化(n=8-10)。 (E)治疗后血糖变化。(F-G)治疗后葡萄糖葡萄糖耐量测试及曲线下面积。(H)血浆胰岛素水平。数据以平均值 ± SEM表示。*p<0.05,**p<0.01,***p<0.001。
GCGR与B-hGCGR mice
GCGR是胰高血糖素的受体,被胰高血糖素激活后,促进糖原分解和糖异生,升高血糖。反之,当GCGR与胰高血糖素被阻断后,则会发挥降低血糖的作用。人源化B-hGCGR小鼠糖尿病模型适用于GCGR相关的小分子拮抗剂、反义寡核苷酸以及抗体等药物的临床前研究。
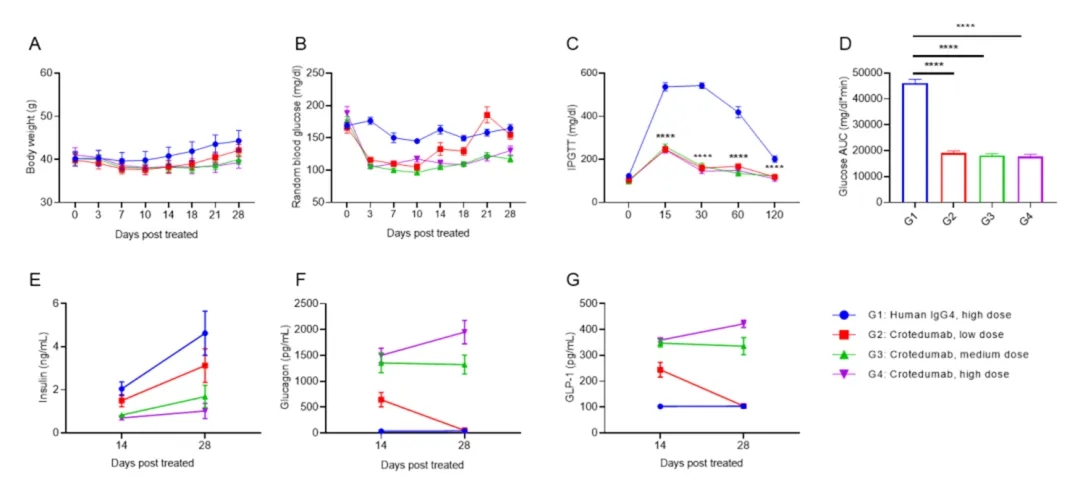 图5:抗人 GCGR 抗体药物crotedumab在HFD诱导的B-hGCGR小鼠中的体内药效研究
图5:抗人 GCGR 抗体药物crotedumab在HFD诱导的B-hGCGR小鼠中的体内药效研究
(A)在饮食诱导后第0天腹腔注射抗人GCGR抗体crotedumab(内部合成)后的体重变化(n=10)。(B)crotedumab给药后随机血糖。(C-D)给药后葡萄糖耐量测试及曲线下面积。(E-G)第14天和第28天的血清胰岛素,胰高血糖素及 GLP-1水平。
GIPR与B-hGIPR mice
胃抑制多肽受体(GIPR)属于g蛋白偶联受体家族。GIPR在许多组织中表达,包括胰腺、胃、脑、肝等。这种蛋白在调节胰岛素分泌、葡萄糖和脂质代谢中起着至关重要的作用。该基因的突变或改变与多种健康状况有关,包括肥胖和糖尿病1、2。GIPR抗体类药物可借助人源化B-hGIPR小鼠进行药效研究。
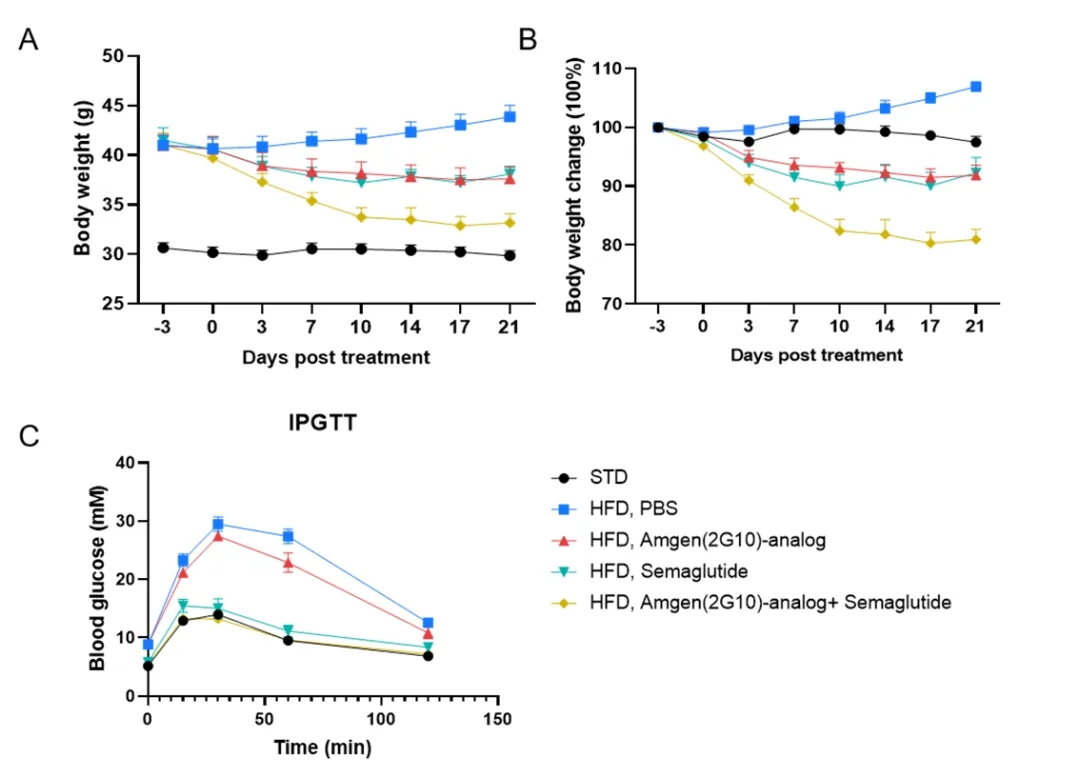
图6:hGIPR抗体Amen(2G10)类似物和Semaglutide在HFD诱导的B-hGIPR小鼠中的体内药效研究
(A-B)HFD诱导12周的B-hGIPR小鼠, Amen(2G10)类似物和Semaglutide治疗后体重变化(n=8)。 (E)治疗后葡萄糖耐受能力。数据以平均值 ± SEM表示。*p<0.05,**p<0.01,***p<0.001。
此外,百奥赛图还提供B-hGIPR/hGLP1R mice、B-hGIPR/hGCGR mice、B-hGLP1R/hGCGR mice以及B-hGCGR/hGIPR/hGLP1R mice等双/多靶点人源化小鼠用于糖尿病及肥胖研究和新药评价。
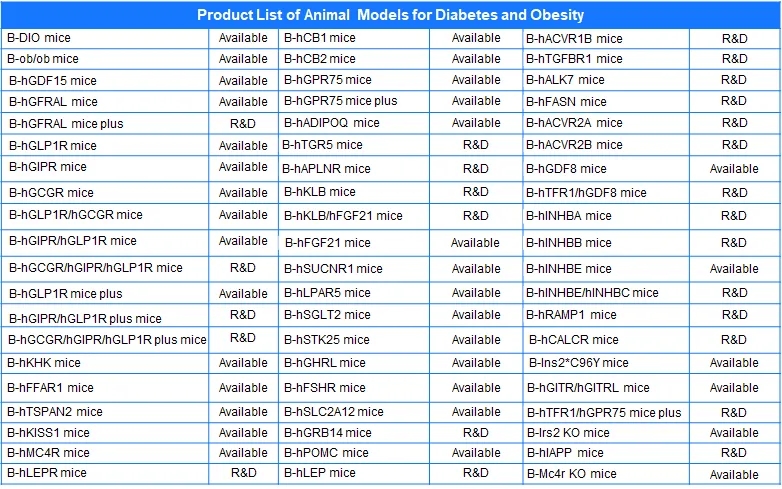
百奥赛图糖尿病及肥胖相关动物模型列表